
Жидкий азот получают из воздуха (атмосферный воздух на 79 % состоит из азота), он нетоксичен, невзрывоопасен.
Физически жидкий азот представляет собой низкотемпературную жидкость с температурой кипения -186°С.
При его использовании следует иметь в виду, что опасным является ожог от прикосновения материала, охлажденного жидким азотом, но кратковременное соприкосновение кожи с жидким азотом не опасно, так как при этом на коже образуется воздушная подушка с низкой теплопроводностью, которая предохраняет кожу от непосредственного контакта с жидким азотом.
Где брать жидкий азот?
Жидкий азот - это побочный продукт при производстве кислорода, поэтому на любой кислородной станции можно найти его в избытке.
Так же он участвует во многих технологических процессах на предприятиях нефтеперерабатывающей, химической, энергетической отраслях и т.д.
Его стоимость в среднем 150 руб. за 1 л.
Как хранить жидкий азот?
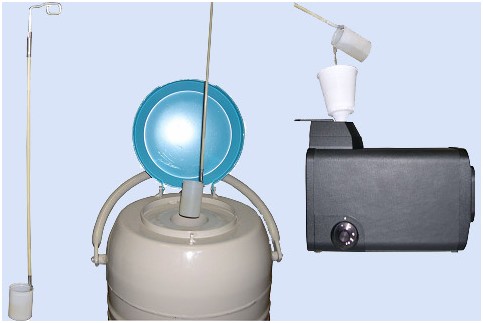
Жидкий азот хранят в специальных сосудах, которые называются сосудами ДЬЮАРА.
Работа с азотом
Жидкий азот желательно заливать в просторном помещении.Необходимо помнить, что избыток азота может вызвать удушье. Поэтому после работы с ним желательно выйти на открытый воздух. Азот имеет очень низкую температуру кипения, поэтому работать желательно втеплых перчатках и желательно не проливать азот на части тела. При вливании азота в колбу(когда она еще не охладилась) происходит резкое выкипание азота с образованием разлетающихся в разные стороны брызг, которых нужно оасаться. Сосуд, в который мы наливаем азот должен обязательно иметь отверстия для выкипания азота при его хранении.
Copyright © 2011 Сергей Матюнин
История открытия
В 1772 году Генри Кавендиш провёл следующий опыт: он многократно пропускал воздух над раскалённым углём, затем обрабатывал его щёлочью, в результате получался остаток, который Кавендиш назвал удушливым (или мефитическим) воздухом. С позиций современной химии ясно, что в реакции с раскалённым углём кислород воздуха связывался в углекислый газ, который затем реагировал со щёлочью. При этом остаток газа представлял собой по большей части азот. Таким образом, Кавендиш выделил азот, но не сумел понять, что это новое вещество. В том же году Кавендиш сообщил об этом Джозефу Пристли.
Пристли в это время проводил серию экспериментов, в которых также связывал кислород воздуха и удалял полученный углекислый газ, то есть также получал азот, однако, будучи сторонником господствующей в те времена теории флогистона, совершенно неверно истолковал полученные результаты (по его мнению, процесс был противоположным — не кислород удалялся из газовой смеси, а наоборот, в результате обжига воздух насыщался флогистоном; оставшийся воздух (азот) он и назвал насыщенным флогистоном, то есть флогистированным). Очевидно, что и Пристли, хотя и смог выделить азот, не сумел понять сути своего открытия, поэтому и не считается первооткрывателем азота.
Одновременно схожие эксперименты с тем же результатом проводил и Карл Шееле.
В 1772 году азот (под названием «испорченного воздуха») как простое вещество описал Даниэль Резерфорд, он опубликовал магистерскую диссертацию, где указал основные свойства азота (не реагирует со щелочами, не поддерживает горения, непригоден для дыхания). Именно Даниэль Резерфорд и считается первооткрывателем азота. Однако и Резерфорд был сторонником флогистонной теории, поэтому также не смог понять, что же он выделил. Таким образом, чётко определить первооткрывателя азота невозможно.
Азот
Азо́т (от греч. ázōos — безжизненный, лат. Nitrogenium), химический символ — N, химический элемент 5-ой группы главной подгруппы 2-го периода периодической системы Менделеева, порядковый номер 7, атомная масса 14,0067
Правила работы с азотом



